Enunciado: Se recogió nitrógeno, N2, por desplazamiento de agua, a 29°C y 807 mmHg. El volumen del gas sobre la superficie del agua fue de 124 ml. Hallar el volumen de gas seco en C. N. Asuma que la presión de vapor del agua a 29 °C es de 30.07 mmHg.
Mas ejercicios resueltos de química
sobre #gases. Mas ejercicios resueltos de otros capítulos
de #química. Curso de #quimicadegases. ¡Si
te gustó, suscríbete!
Demostración
de las ecuaciones clave:
https://quimicadejoseleg-lamateria.blogspot.com/2021/06/la-ley-de-dalton-de-presiones-parciales.html
Solución:
El volumen de gases involucrados es una mezcla, por ende, aplicamos la ley de Dalton.
Si asumimos que la sustancia (i) es el nitrógeno y la sustancia (ii) es el agua, entonces podemos calcular la presión parcial del gas seco en las condiciones iniciales.
Las demás propiedades de la mezcla como 124 ml y 29 °C las mantendremos para el nitrógeno seco. Este volumen cambiará cuando las condiciones cambien, por lo que tendremos que calcular el volumen final. Para esto iniciamos con la ley de gases ideales, asumimos que no hay escapes de gas, por lo que fusionamos n y R. Luego dividimos la ecuación entre los términos iniciales que permiten cancelar la constante, y final mente despejamos el volumen final.
Igualamos las dos expresiones para obtener la solución analítica final.
Reemplazamos teniendo en cuenta que en CN la presión es 760 mmHg y la temperatura 273.15 K
Otros
enunciados: como hallar el volumen de gas seco con la presión de vapor y la ley de dalton, como usar la ley de dalton
y la presión de vapor del agua para calcular el volumen de gas seco, si
conocemos la presión de vapor y la ley de dalton como calcular el volumen de
gas seco, como calcular el volumen de N2 seco con el volumen de aire desplazado,
Hallar el volumen de gas seco en CN, hallar el volumen de gas seco en stp, Hallar
el volumen de gas seco en tps


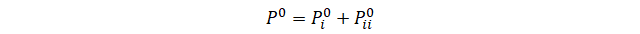




No hay comentarios:
Publicar un comentario