👉Enunciado: Cierto día, un barómetro de laboratorio indica que la presión atmosférica es de 764.7 torr. Se coloca una muestra de gas en un matraz unido a un manómetro de mercurio de extremo abierto y se usa una varilla de medición para medir la altura del mercurio en los dos brazos del tubo en U. La altura del mercurio en el brazo del extremo abierto es de 136.4 mm y la altura del brazo en contacto con el gas en el matraz es de 103.8 mm. ¿Cuál es la presión del gas en el matraz (a) en atmósferas, (b) en kilopascales?
|| Enlace a YouTube || Mas
ejercicios resueltos || Ejercicios
de otros capítulos de química || Química
de gases || ¡Si te gustó, suscríbete! ||
👉Demostración de las ecuaciones clave:
https://quimicadejoseleg-lamateria.blogspot.com/2022/01/barometro-manometro-aire-peso.html
👉Solución:
Asumiremos un manómetro, es decir un tubo en U con un brazo abierto que
denominaremos como columna 2 o h2, y un extremo cerrado y conectado a un matraz
redondo que denominaremos columna 1 o h1.
🤖 Literal (a):
El modelo
matemático para esta situación fue planteado en el enlace anterior, el cual
expresa que a diferencia de lo que plantea el libro de texto, lo que debemos
hacer es sacar la diferencia entre la altura de ambas columnas:
Adicionalmente tenga en cuenta que una atmósfera equivale a 760 torricellis y también milímetros de mercurio, por lo que torr = mmHg = 760-1 atm.
🤖 Literal (b):
Dado que 1 atm = 101 325 Pa, si movemos la coma en los pascales tres posiciones a la izquierda, obtendremos kilo pascales: 1 atm = 101.325 kPa y reemplazamos algebraicamente en la solución del literal (a):
👉Otros
enunciados: Determine la presión de un gas empleando un manómetro U con 136.4 y
103.8 mmHg, Determinar la presión de un gas empleando un manómetro U con 136.4
y 103.8 mmHg, Halle la presión de un gas empleando un manómetro U con 136.4 y
103.8 mmHg, Hallar la presión de un gas empleando un manómetro U con 136.4 y
103.8 mmHg, Calcule la presión de un gas empleando un manómetro U con 136.4 y
103.8 mmHg, Calcular la presión de un gas empleando un manómetro U con 136.4 y
103.8 mmHg,
👉Temas: química, química general, química de gases,
barómetro de Torricelli, el manómetro, joseleg



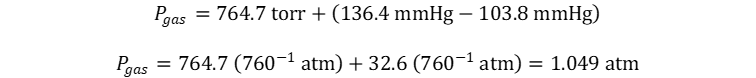

No hay comentarios:
Publicar un comentario