👉Enunciado: Una muestra de 2.14 L de gas cloruro de hidrógeno (HCl) a 2.61 atm y 28 ° C se disuelve completamente en 668 mL de agua para formar una solución de ácido clorhídrico. Calcula la molaridad de la solución ácida. Suponga que no hay cambios en el volumen.
|| Enlace a YouTube || Mas
ejercicios resueltos || Ejercicios
de otros capítulos de química || Química
de gases || ¡Si te gustó, suscríbete! ||
👉Demostración
de las ecuaciones clave:
https://quimicadejoseleg-lamateria.blogspot.com/2022/01/intro-concentracion-gases.html
👉Solución: Emplearemos la solución analítica que dedujimos en este enlace (Enlace→)
Donde (V(ac)) es el volumen total de la
disolución líquida o acuosa que es la suma del aporte en volumen líquido del agua (que
denominaremos sustancia ii) y el HCl. En este caso asumiremos a priori
que el HCl no afecta significativamente a (V(ac)), por lo que
el volumen de la disolución es igual al volumen de agua (V(ac)
= Vii).
Reemplazamos.
Tenga en cuenta que este ejercicio nos induce al error de calcular la molaridad de un gas, donde despejamos el cociente (ni/Vi) de la ecuación de estado. En mi país, a ejercicios maliciosos como este los denominamos la cascara de banano, o simplemente la cascarita.
👉Otros enunciados: Determine la
molaridad de HCl acuoso si 2.14 L 2.61 atm 28 ° C se disuelven en 668 mL, Determinar la molaridad de HCl acuoso si 2.14 L 2.61 atm 28 ° C se
disuelven en 668 mL, Calcule la molaridad de HCl
acuoso si 2.14 L 2.61 atm 28 ° C se disuelven en 668 mL, Calcular la molaridad de HCl acuoso si 2.14 L 2.61 atm 28 ° C se
disuelven en 668 mL, Halle la molaridad de HCl
acuoso si 2.14 L 2.61 atm 28 ° C se disuelven en 668 mL, Hallar la molaridad de HCl acuoso si 2.14 L 2.61 atm 28 ° C se
disuelven en 668 mL,
👉Temas: química, química general, química de gases,
leyes de los gases, ecuación de estado, concentración molar de un gas,
diferencia entre la molaridad de un gas y una disolución líquida, joseleg




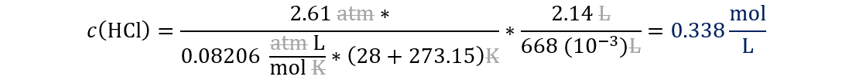
No hay comentarios:
Publicar un comentario