👉Enunciado: Una muestra de 6.0 L a 25 ° C y 2.00 atm de presión contiene 0.5 mol de gas. Si se agrega gas hasta completar 0.75 moles a la misma presión y temperatura, ¿cuál es el volumen total final del gas?
|| Enlace a YouTube || Mas
ejercicios resueltos || Ejercicios
de otros capítulos de química || Química
de gases || ¡Si te gustó, suscríbete! ||
👉Demostración
de las ecuaciones clave:
https://quimicadejoseleg-lamateria.blogspot.com/2021/06/la-ley-molar-de-avogadro.html
👉Solución: Usaremos la forma dinámica de Avogadro para cambio de estado, y despejamos el volumen final.
Reemplazamos
👉Otros
enunciados: determine el volumen final de un gas a 0.5 mol y 6 L que pasa a tener
0.75 moles, Determinar el volumen final de un gas a 0.5 mol y 6 L que pasa a
tener 0.75 moles, calcule el volumen final de un gas a 0.5 mol y 6 L que pasa a
tener 0.75 moles, Calcular el volumen final de un gas a 0.5 mol y 6 L que pasa
a tener 0.75 moles, Halle el volumen final de un gas a 0.5 mol y 6 L que pasa a
tener 0.75 moles, Hallar el volumen final de un gas a 0.5 mol y 6 L que pasa a
tener 0.75 moles,
👉Temas: química, química general, química de gases,
leyes de los gases, ecuación de estado, ley de Avogadro, joseleg



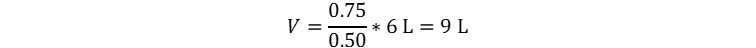
No hay comentarios:
Publicar un comentario