👉Enunciado: Calcular el volumen de oxígeno requerido para completar la combustión de 0.25 dm3 de metano, teniendo en cuenta la ecuación química: CH4 + 2O2 → CO2 + 2H2O.
|| Enlace a YouTube || Mas
ejercicios resueltos || Ejercicios
de otros capítulos de química || Química
de gases || ¡Si te gustó, suscríbete! ||
👉Demostración
de las ecuaciones clave:
https://quimicadejoseleg-lamateria.blogspot.com/2022/01/ley-volumenes-combinacion-gases.html
👉Solución: Usaremos
la ley de volúmenes de combinación, despejando el volumen de la sustancia
incógnita.
Reemplazamos asumiendo que la sustancia (i) es oxígeno y la sustancia (d) es el metano.
👉Otros
enunciados: Halle el volumen de O2 que consume completamente 0.25 dm3 de metano,
Hallar el volumen de O2 que consume completamente 0.25 dm3 de metano, Determine
el volumen de O2 que consume completamente 0.25 dm3 de metano, Determinar el
volumen de O2 que consume completamente 0.25 dm3 de metano, Calcule el volumen
de O2 que consume completamente 0.25 dm3 de metano, Calcular el volumen de O2
que consume completamente 0.25 dm3 de metano,
👉Temas: química, química general, química de gases,
leyes de los gases, ecuación de estado, ley de Gay-Lussac de volúmenes de
combinación, joseleg



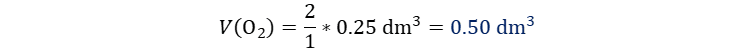
No hay comentarios:
Publicar un comentario