👉Enunciado: Obtener la ley de los gases ideales a partir de las leyes empíricas de los gases.
|| Enlace a YouTube || Mas
ejercicios resueltos || Ejercicios
de otros capítulos de química || Química
de gases || ¡Si te gustó, suscríbete! ||
👉Demostración
de las ecuaciones clave:
https://quimicadejoseleg-lamateria.blogspot.com/2022/01/Historia-quimica-gases.html
👉Solución: No necesitamos hacer la demostración a partir de todas las leyes de los gases, solo necesitamos multiplicar la ley de Avogadro por la ley de Gay-Lussac ya que estas dos son las que contienen todas las propiedades de los gases que necesitamos en la ecuación de estado.
Multiplicar
dos ecuaciones es sencillo, ya que ambos lados de la operación son
independientes. En este caso dejamos las constantes al interior de un
paréntesis. De esta manera a la izquierda tenemos el producto de presión y
volumen, y a la derecha tenemos el producto de las constantes, por cantidad de
sustancia, por temperatura, una estructura muy semejante a la que estamos
buscando.
El producto de dos constantes es una nueva constante, que en este caso es la constante de los gases ideales, y reorganizamos para que la ecuación quede elegante.
👉Otros
enunciados: Demostrar la le ecuación de estado a partir de la ley de Avogadro y la
ley de Gay-Lussac,
👉Temas: química, química general, química de gases,
leyes de los gases, ecuación de estado, joseleg



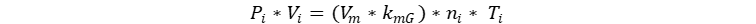

No hay comentarios:
Publicar un comentario