👉Enunciado: Hallar el valor de la constante en la ley de Avogadro (volumen molar) a 1.00 atm y 273 K de gas ideal y hacer el dibujo de la gráfica.
|| Enlace a YouTube || Mas
ejercicios resueltos || Ejercicios
de otros capítulos de química || Química
de gases || ¡Si te gustó, suscríbete! ||
👉Demostración
de las ecuaciones clave:
https://quimicadejoseleg-lamateria.blogspot.com/2021/06/la-ley-molar-de-avogadro.html
👉Solución: La
forma estática de la ley de Avogadro establece que:
Pero este en enunciado no nos ofrece ni el volumen o
los moles. Lo que vamos a hacer es despejar el volumen molar.
Y despejamos el mismo cociente volumen sobre
temperatura de la ley de los gases ideales.
Por lo que el volumen molar es:
Por tanto:
Por lo tanto, por cada mol que aumenta, el volumen
aumenta 22.4 L y viceversa, lo cual nos permite dibujar una gráfica de la ley
de Avogadro como se muestra en el video.
👉Otros enunciados: como se grafica la ley de Avogadro, como calcular la constante de la ley de Avogadro, que necesito para graficar la ley de Avogadro, como dibujo la gráfica de la ley de Avogadro, como hallar el volumen molar, que es 22.4 L/mol
👉Temas: química, química general, química de gases,
leyes de los gases, ecuación de estado, ley de Avogadro, joseleg



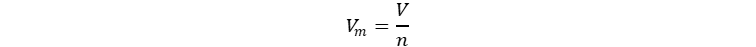




No hay comentarios:
Publicar un comentario