👉Enunciado: La azida de sodio (NaN3) se usa en algunas bolsas de aire de automóviles. El impacto de una colisión desencadena la descomposición del NaN3 de la siguiente manera: 2NaN3 (s) → 2Na (s) + 3N2 (g). El gas nitrógeno producido infla rápidamente la bolsa entre el conductor y el parabrisas y el tablero. Calcule el volumen de N2 generado a 80 °C y 823 mmHg por la descomposición de 60.0 g de NaN3.
|| Enlace a YouTube || Mas ejercicios
resueltos || Ejercicios
de otros capítulos de química || Química
de gases || ¡Si te gustó, suscríbete! ||
👉Demostración de las ecuaciones clave:
https://quimicadejoseleg-lamateria.blogspot.com/2022/01/estequiometria-gases.html
👉Solución: Este es un problema volumen a volumen, por lo que emplearemos la ley de volúmenes de combinación de Gay-Lussac. El volumen del dato lo reemplazamos por lo que vale en términos de variables de gas (despejando volumen de P V = n R T). Finalmente reemplazamos cantidad de sustancia (n) por el cociente masa sobre la masa molar (m/M).
El dato es (NaN3), por lo que calculamos su masa molar.
Reemplazamos en la
solución analítica.
👉Otros enunciados: Determine el volumen
de N2 generado a 80 °C y 823 mmHg por 60.0 g de NaN3,
Determinar el volumen de N2 generado a 80 °C y 823 mmHg por
60.0 g de NaN3, Calcule el volumen de N2 generado a 80 °C y 823 mmHg por 60.0 g de NaN3,
Calcular el volumen de N2 generado a 80 °C y 823 mmHg por
60.0 g de NaN3, Halle el volumen de N2 generado
a 80 °C y 823 mmHg por 60.0 g de NaN3, Hallar el volumen
de N2 generado a 80 °C y 823 mmHg por 60.0 g de NaN3,
👉Temas: química, química general, química de gases,
leyes de los gases, ecuación de estado, estequiometría de gases, estequiometría
de gases volumen a volumen, volúmenes de combinación de Gay-Lussac, joseleg




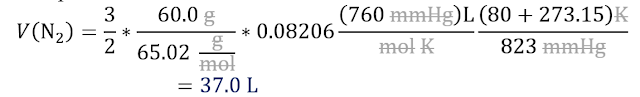
No hay comentarios:
Publicar un comentario