👉Enunciado: Suponiendo que no hay cambios en la temperatura y la presión, calcule el volumen de O2 (en litros) necesario para la combustión completa de 14.9 L de butano (C4H10): 2C4H10 (g) + 13O2 (g) → 8CO2 (g) + 10H2O (l)
|| Enlace a YouTube || Mas
ejercicios resueltos || Ejercicios
de otros capítulos de química || Química
de gases || ¡Si te gustó, suscríbete! ||
👉Demostración
de las ecuaciones clave:
https://quimicadejoseleg-lamateria.blogspot.com/2022/01/estequiometria-gases.html
👉Solución: Este es un problema volumen a volumen, por lo que emplearemos la ley de volúmenes de combinación de Gay-Lussac.
Reemplazamos
teniendo en cuenta que la sustancia (i) es el oxígeno y la sustancia (d) es el butano
y los números estequiométricos: 2C4H10
(g) + 13O2 (g) → 8CO2 (g) + 10H2O (l).
👉Otros
enunciados: Determine el volumen de O2 que consume completamente 14.9 L de butano,
Determinar el volumen de O2 que consume completamente 14.9 L de butano, Calcule
el volumen de O2 que consume completamente 14.9 L de butano, Calcular el
volumen de O2 que consume completamente 14.9 L de butano, Halle el volumen de
O2 que consume completamente 14.9 L de butano, Hallar el volumen de O2 que
consume completamente 14.9 L de butano,
👉Temas: química, química general, química de gases,
leyes de los gases, ecuación de estado, estequiometría de gases, estequiometría
de gases volumen a volumen, volúmenes de combinación de Gay-Lussac, joseleg



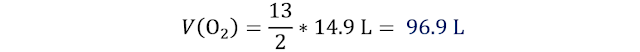
No hay comentarios:
Publicar un comentario